üĒį┤Ż║ŠW(w©Żng)Įj(lu©░)┘Yį┤ 2023-03-22 17:52:24
│§ųą╗»īW(xu©”)╚▄ĮŌČ╚Ū·ŠĆĮŌøQĘĮĘ©
╚▄ĮŌČ╚Ū·ŠĆĄ─æ¬(y©®ng)ė├
ę╗Īó
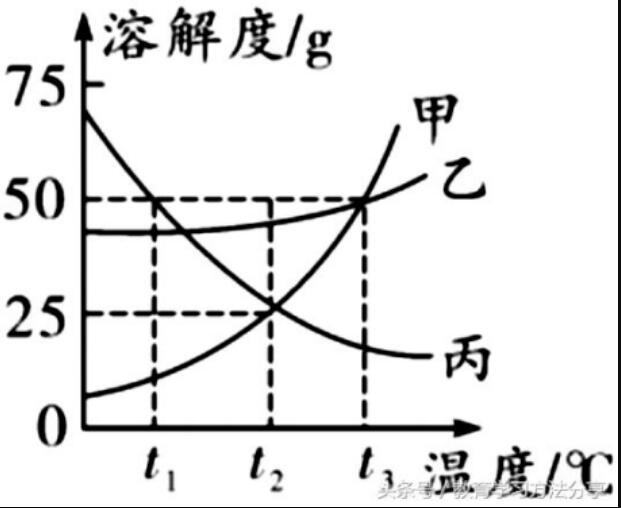
1.šę╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚
├žšą
įō╬’┘|(zh©¼)į┌─│ę╗£žČ╚Ž┬Ū·ŠĆ╔Ž³cī”æ¬(y©®ng)Ą─┐vū°ś╦(bi©Īo)ųĄŻ¼╚ń▒¹╬’┘|(zh©¼)į┌t1ĪµĢrĄ─╚▄ĮŌČ╚×ķ50 gĪŻ
2.▒╚▌^▓╗═¼╬’┘|(zh©¼)į┌═¼ę╗£žČ╚Ž┬╚▄ĮŌČ╚Ą─┤¾ąĪ
├žšą
═¼ę╗£žČ╚Ž┬Ż¼╬╗ė┌╔ŽĘĮŪ·ŠĆī”æ¬(y©®ng)╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚┤¾ė┌Ž┬ĘĮŪ·ŠĆī”æ¬(y©®ng)╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚ĪŻ╚ń0 ~t3ĪµŻ¼ęęĄ─Ū·ŠĆį┌╝ūĄ─╔ŽĘĮŻ¼╚▄ĮŌČ╚┤¾ąĪ×ķęę>╝ū;0 ~ t2ĪµŻ¼▒¹Ą─Ū·ŠĆį┌╝ūĄ─╔ŽĘĮŻ¼╚▄ĮŌČ╚┤¾ąĪ×ķ▒¹>╝ū;t2ĪµĢrŻ¼╝ūĪó▒¹ā╔Ū·ŠĆŽÓĮ╗Ż¼┤╦Ģr╚▄ĮŌČ╚┤¾ąĪ×ķ╝ū=▒¹ĪŻ
╠žäe╠ßąčŻ║▒╚▌^╚▄ĮŌČ╚Ż¼£žČ╚╩ŪŪ░╠ß
3.┼ąöÓ╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚ļS£žČ╚ūā╗»Ą─┌ģä▌
├žšą
Ęų╬÷╚▄ĮŌČ╚Ū·ŠĆĄ─Ų┬Č╚╝░ū▀Ž“Ż¼Å─ū¾Ž“ėę┐┤Ū·ŠĆĄ─ū▀ä▌╩ŪŽ“╔ŽĪóŽ“Ž┬▀Ć╩ŪŲĮŠÅĪŻ│ŻęŖ╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚Ū·ŠĆ┐╔Ęų×ķŻ║
ČĖ╔²ą═
1.Ż║▒Ē╩Š╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚ļS£žČ╚╔²Ė▀├„’@į÷┤¾Ż¼╚ń╝ū;
ŠÅ╔²ą═
2.Ż║▒Ē╩Š╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚ļS£žČ╚Ą─╔²Ė▀į÷┤¾▓╗├„’@Ż¼╚ńęę;
Ž┬ĮĄą═
3.Ż║▒Ē╩Š╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚ļS£žČ╚Ą─╔²Ė▀Č°Ž┬ĮĄŻ¼╚ń▒¹ĪŻ
4.’¢║═╚▄ę║┼c▓╗’¢║═╚▄ę║Ą─┼ąöÓ┼c▐D(zhu©Żn)╗»
├žšą
ęį╚▄ĮŌČ╚Ū·ŠĆ×ķĮńŽ▐Ż¼Ū·ŠĆ╔Ž╝░╔ŽĘĮĄ─³c┤·▒Ēįō╬’┘|(zh©¼)ī”æ¬(y©®ng)£žČ╚Ž┬Ą─’¢║═╚▄ę║Ż¼Ū·ŠĆŽ┬ĘĮĄ─³c┤·▒Ēįō╬’┘|(zh©¼)ī”æ¬(y©®ng)£žČ╚Ž┬Ą─▓╗’¢║═╚▄ę║ĪŻī”ė┌’¢║═╚▄ę║┼c▓╗’¢║═╚▄ę║Ą─▐D(zhu©Żn)╗»ĘĮĘ©╚ńŽ┬Ż║
a. ī”ė┌┤¾ČÓöĄ(sh©┤)╣╠¾w(╚▄ĮŌČ╚ļS£žČ╚╔²Ė▀Č°į÷┤¾Ą─╬’┘|(zh©¼))Ż║
b. ī”ė┌śO╔┘öĄ(sh©┤)╣╠¾w(╚▄ĮŌČ╚ļS£žČ╚╔²Ė▀Č°£pąĪĄ─╬’┘|(zh©¼))Ż║
ó▌╚▄ę║ųą╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)Ą─ėŗ╦Ń╝░┤¾ąĪ▒╚▌^
├žšą
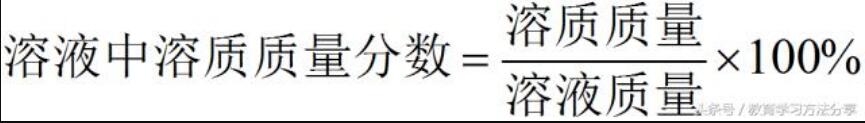
Ż¼
╚¶╚▄ę║×ķ’¢║═╚▄ę║Ż¼ätŻ║

Ż¼
═©▀^ėŗ╦Ń┐╔▒╚▌^╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)Ą─┤¾ąĪĪŻī”ė┌’¢║═╚▄ę║Ą─╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)ėąŻ║«ö(d©Īng)0< t < t3ĢrŻ¼╝ūĪóęęā╔ĘN’¢║═╚▄ę║Ą─╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)×ķęę>╝ū;«ö(d©Īng)t = t3ĢrŻ¼╝ūĪóęęā╔ĘN’¢║═╚▄ę║Ą─╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)ŽÓĄ╚;t > t3ĢrŻ¼╝ūĪóęęā╔ĘN’¢║═╚▄ę║Ą─╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)×ķ╝ū>ęęĪŻ
ó▐£žČ╚ūā╗»Ģr╚▄ę║┘|(zh©¼)┴┐Īó╚▄ä®┘|(zh©¼)┴┐Īó╚▄┘|(zh©¼)┘|(zh©¼)┴┐╝░╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)Ą─ūā╗»
├žšą1
Ė∙ō■(j©┤)ėą¤oŠ¦¾w╬÷│÷
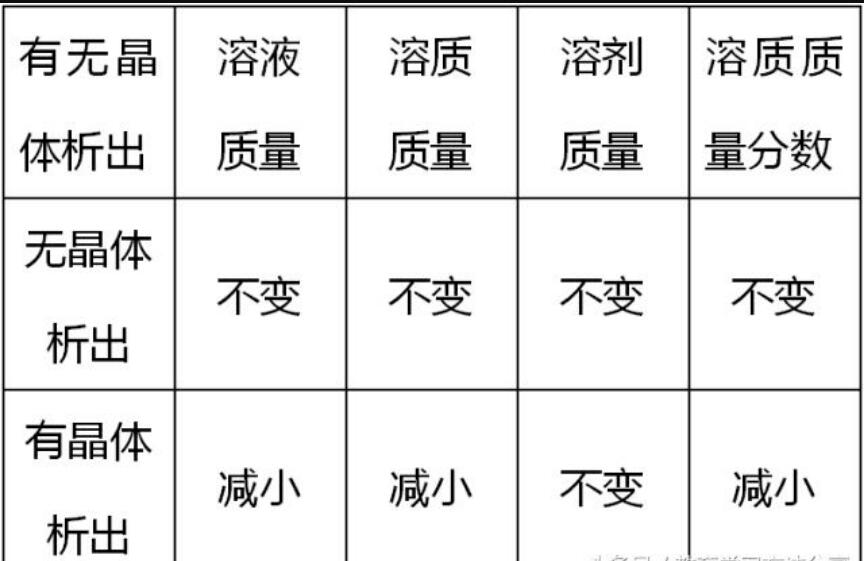
├žšą2
Ė∙ō■(j©┤)Ū·ŠĆū▀Ž“(’¢║═╚▄ę║▀mė├)

ó▀┼ąöÓ╬’┘|(zh©¼)ĮY(ji©”)Š¦╗“╠ß╝āĄ─ĘĮĘ©
├žšą
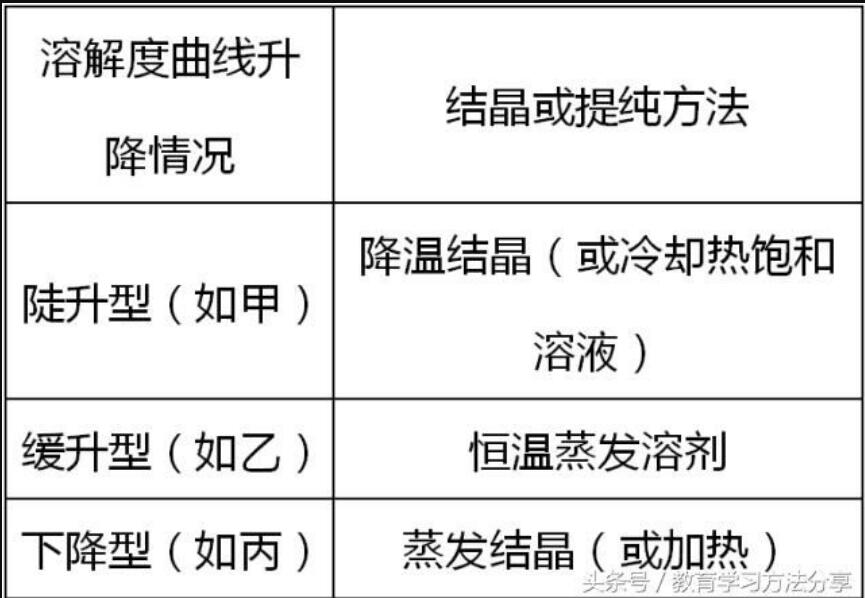
Č■Īó╚▄ĮŌČ╚▒Ē
Ž┬▒Ē╩ŪKCl║═KNO3į┌▓╗═¼£žČ╚Ž┬Ą─╚▄ĮŌČ╚ĪŻ
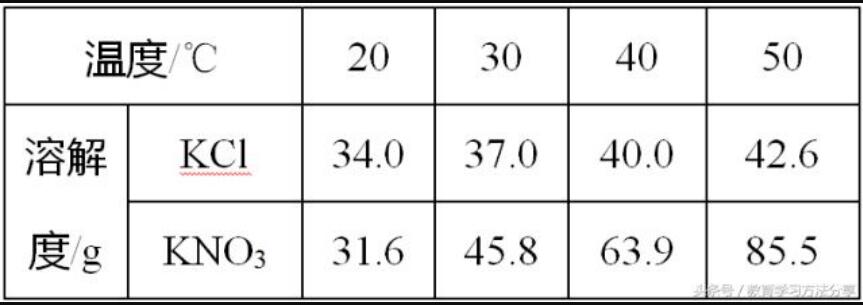
┼ąöÓā╔ĘN╬’┘|(zh©¼)Ą─╚▄ĮŌČ╚ūā╗»┌ģä▌║═ā╔╬’┘|(zh©¼)╚▄ĮŌČ╚ŽÓĄ╚Ą─£žČ╚ĘČć·ĪŻ
├žšą
ĮŌøQ▀@ŅÉå¢Ņ}Ż¼┐╔ęį═©▀^ī”▒╚═¼ę╗╬’┘|(zh©¼)į┌▓╗═¼£žČ╚Ą─╚▄ĮŌČ╚ūā╗»Ż¼Å─Č°┼ąöÓ╬’┘|(zh©¼)╚▄ĮŌČ╚Ą─ūā╗»┌ģä▌ĪŻ═©▀^▒╚▌^ā╔╬’┘|(zh©¼)į┌═¼ę╗£žČ╚Ą─╚▄ĮŌČ╚┤¾ąĪŻ¼╚ń20ĪµĢrŻ¼KClĄ─╚▄ĮŌČ╚┤¾ė┌KNO3Ą─╚▄ĮŌČ╚Ż¼30ĪµĢrŻ¼KNO3Ą─╚▄ĮŌČ╚┤¾ė┌KClĄ─╚▄ĮŌČ╚Ż¼╣╩į┌20Īµ~30ĪµĄ──│ę╗£žČ╚Ž┬Ż¼Č■š▀Ą─╚▄ĮŌČ╚ŽÓĄ╚ĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖC(j©®)ĪóŲĮ░ÕĄ╚ęŲäėįO(sh©©)éõįLå¢ųą┐╝ŠW(w©Żng)Ż¼2025ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³cō¶▓ķ┐┤